Условия образования водородной связи между атомами
Внешний вид

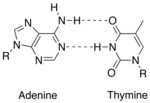

Водородная связь (hydrogen bonds) образуется когда:
- расстояние |D-A| < dist = 3
- угол D-H-A < ang = 20°
- C-G
- N-H — O
- N — H-N
- O — H-N
- T(U)-A
- O — H-N
- N-H — N
Итого без учета угла:
- H-O (O-H) 1.38-1.56
- H-N (N-H) 1.44-1.56
- G-U (A-C)
- N-H — O
- O — H-N
Почему связи типа водородных не образуют атомы других элементов?
[править]Силы электростатического притяжения диполей полярных связей (О-Н, N-H и т.п.) слабы и действуют лишь на малых расстояниях. Водород, обладая наименьшим атомным радиусом, позволяет сблизиться таким диполям настолько, что силы притяжения становятся заметными. Никакой другой элемент с большим атомным радиусом не способен к образованию водородных связей.
